Generel information
Androgen biosyntesehæmmer.
Anvendelsesområder
Hos voksne mænd i kombination med prednison eller prednisolon til:
- Nydiagnosticeret, metastaserende hormonfølsom prostatacancer (mHSPC) i kombination med androgen deprivationsbehandling (ADT).
- Nydiagnosticeret, ikke-metastaserende hormonfølsom prostatacancer (HSPC) med høj risiko i kombination med androgen deprivationsbehandling (ADT) og strålebehandling.
- Metastaserende kastrationsresistent prostatacancer(mCRPC), som er asymptomatisk eller med lette symptomer, efter svigt af androgen deprivationsbehandling og hvor kemoterapi endnu ikke er klinisk indiceret.
- Metastaserende kastrationsresistent prostatacancer (mCRPC) med progression af sygdommen under eller efter kemoterapi med docetaxel.
Ved HSPC anbefales behandling indtil sygdomsprogression, uacceptabel toksicitet eller i op til 2 år hos patienter uden sygdomsprogression. Ved øvrige indikationer anbefales behandling indtil sygdomsprogression eller uacceptabel toksicitet.
Abirateron bør kun anvendes, når behandlingen forestås af læger med særligt kendskab til maligne lidelser og deres behandling.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 500 mg abirateronacetat.
Doseringsforslag
Voksne
- 1.000 mg 1 gang dgl.
- Anvendes i kombination med prednison eller prednisolon (5 mg dgl. ved HSPC og 10 mg dgl. ved mCRPC).
- Medicinsk kastration med GnRH-analog bør fortsætte under behandlingen.
Håndtering af kapsler og tabletter
| filmovertrukne tabletter 500 mg, Medical Valley Ingen kærv |
Mad og drikke
Tages med et glas vand.
Tages på tom mave mindst 1 time før eller mindst 2 timer efter et måltid.
Knusning/åbning
Må ikke knuses.
Administration
Synkes hele.
Se endvidere Håndtering af tabletter og kapsler.
Nedsat leverfunktion
- Behandling bør overvejes nøje ved moderat nedsat leverfunktion (Child-Pugh B). Behov for dosisjustering kan ikke forudses.
- Kontraindiceret ved stærkt nedsat leverfunktion (Child-Pugh C).
Forsigtighedsregler
- CYP17-hæmning medfører øget produktion af mineralokortikoid i binyrerne med risiko for hypertension, hypokaliæmi og væskeretention, og forsigtighed tilrådes ved aktuel eller tidligere kardiovaskulær sygdom. Ved væsentlig risiko for kongestiv hjerteinsufficiens bør kontrol foretages hver 2. uge i de første 3 måneder og derefter hver måned. Under behandlingen skal der holdes øje med udvikling af hypertension, hypokaliæmi og ødemer.
- Kontrol af aminotransferaser bør foretages før behandlingsstart, hver 2. uge i de første 3 mdr. og herefter 1 gang om måneden. Behandlingen seponeres ved aminotransferaser > 5 gange øverste normalgrænse. Efter fald til baselineniveau af leverfunktionsprøverne kan behandlingen genoptages med halv dosis, og levertal bør så kontrolleres hver 2. uge i 3 mdr. og derefter månedligt. Opstår der på ny levertoksicitet, seponeres behandlingen.
- Hvis ALAT har været ≥ 20 gange øverste normalgrænse, bør behandlingen ikke genoptages.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Meget almindelige (> 10 %) | ||
| Mave-tarm-kanalen | Diarré | |
| Metabolisme og ernæring | Hypokaliæmi | |
| Nyrer og urinveje | Urinvejsinfektion | |
| Vaskulære sygdomme | Hypertension, Perifere ødemer | |
| Almindelige (1-10 %) | ||
| Hjerte | Angina pectoris, Arytmier, Atrieflimren, Hjerteinsufficiens | Takykardi |
| Mave-tarm-kanalen | Dyspepsi | |
| Infektioner og parasitære sygdomme | Sepsis | |
| Undersøgelser | Forhøjede levertransaminaser | |
| Metabolisme og ernæring | Hypertriglyceridæmi | |
| Knogler, led, muskler og bindevæv | Øget risiko for knoglebrud | |
| Nyrer og urinveje | Hæmaturi | |
| Hud og subkutane væv | Hududslæt | |
| Ikke almindelige (0,1-1 %) | ||
| Metabolisme og ernæring | Binyrebarkinsufficiens | |
| Knogler, led, muskler og bindevæv | Myopati, Rhabdomyolyse | |
| Sjældne (0,01-0,1 %) | ||
| Lever og galdeveje | Fulminant hepatitis | |
| Luftveje, thorax og mediastinum | Allergisk alveolitis | |
| Ikke kendt hyppighed | ||
| Hjerte | Myokardieinfarkt | |
| Immunsystemet | Anafylaktisk reaktion | |
| Undersøgelser | Forlænget QT-interval | |
Interaktioner
- Abirateron hæmmer CYP2D6 og CYP2C8. Forsigtighed tilrådes, når abirateron anvendes sammen med lægemidler, der aktiveres eller metaboliseres af CYP2D6 eller CYP2C8 - især lægemidler med snævert terapeutisk indeks, fx klasse 1C-antiarytmika (flecainid og propafenon) og tricykliske antidepressiva.
- Stærke CYP3A4-hæmmere og -induktorer skal anvendes med forsigtighed. Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
- Generel forsigtighed ved samtidig behandling med midler, der kan forlænge QTc-intervallet - bl.a. lithium, visse antiarytmika (fx sotalol), visse makrolider (fx erythromycin), visse antidepressiva (fx citalopram, escitalopram) og visse antipsykotika (fx quetiapin). Se endvidere Antiarytmika.
- Spironolacton kan øge koncentrationen af prostataspecifikt antigen (biomarkør for prostatacancer).
Graviditet
Ikke indiceret til kvinder.
Se også Klassifikation - graviditet
Fertile kvinder og mænd
Patienten skal anvende kondom, hvis partneren er gravid.
Kvindelige partnere i den fertile alder skal yderligere anvende anden sikker kontraception.
Amning
Bloddonor
Alkohol
Alkohol og Abirateron "Medical Valley" påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
Hæmmer biosyntesen af testosteron i testikler, binyrer og tumorvæv ved blokering af enzymet CYP17, der katalyserer konverteringen af pregnenolon og progesteron til testosteronforstadierne DHEA og androstenedion.
Farmakokinetik
- Maksimal plasmakoncentration efter ca. 2 timer indtaget fastende.
- Absorptionen øges ved samtidig fødeindtagelse, og abiratonacetat må ikke indtages samtidig med føde.
- Plasmahalveringstid ca. 15 timer.
- Udskilles hovedsageligt med fæces.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Udvalgte hjælpestoffer |
|---|---|---|---|
| filmovertrukne tabletter | 500 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (BEGR) | filmovertrukne tabletter
500 mg
Abirateron "Medical Valley" |
167067 |
56 stk. (blister)
|
Udgået 23-06-2025 |
Substitution
| filmovertrukne tabletter 500 mg |
|---|
| Abirateron "Sandoz" Sandoz, Abirateron, filmovertrukne tabletter 500 mg |
| Abiraterone "Accord" Accord, Abirateron, filmovertrukne tabletter 500 mg |
| Abiraterone "Glenmark" Glenmark Nordic, Abirateron, filmovertrukne tabletter 500 mg |
| Abiraterone "Stada" STADA Nordic, Abirateron, filmovertrukne tabletter 500 mg |
| Abiraterone "Zentiva" Zentiva, Abirateron, filmovertrukne tabletter 500 mg |
| Zytiga Janssen, Abirateron, filmovertrukne tabletter 500 mg |
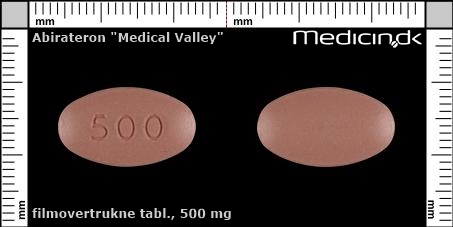
Foto og identifikation
Filmovertrukne tabletter 500 mg |
| Præg: |
500
|
| Kærv: | Ingen kærv |
| Farve: | Rosa |
| Mål i mm: | 11 x 19 |
Referencer
3800. pro.medicin.dk. 2025, https://pro.medicin.dk/ (Lokaliseret 5. maj 2025)
3801. Drugs.com. 2025, https://www.drugs.com/ (Lokaliseret 5. maj 2025)
1550. SPC, Lægemiddelstyrelsen. , http://www.produktresume.dk (Lokaliseret 17. marts 2023)
3802. Micromedex. , https://www.micromedexsolutions.com (Lokaliseret 5. maj 2025)
3803. Produktresumeer. http://www.produktresume.dk, http://www.ema.europa.eu, https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm, https://www.medicines.org.uk. , (Lokaliseret 5. maj 2025)
3966. SPC, EMA. European Medicines Agency. , https://www.ema.europa.eu/en/medicines (Lokaliseret 6. februar 2024)



