Yderligere information
Calciumantagonist (gruppe II) med overvejende kardilaterende virkning. Middel mod angina pectoris. Antihypertensivum.
Anvendelsesområder
- Stabil angina pectoris
- Prinzmetals angina
- Arteriel hypertension
- Raynauds syndrom.
Andre anvendelsesområder
Dispenseringsform
Depottabletter. 1 depottablet (filmovertrukken) indeholder 30 mg nifedipin.
Doseringsforslag
Voksne
Angina pectoris og hypertension
- 20-120 mg 1 gang dgl.
Raynauds syndrom
- 20-120 mg 1 gang dgl.
Bemærk:
- Lavere vedligeholdelsesdosis kan være nødvendig ved ældre patienter > 65 år.
- Begrænset erfaring vedr. børn og unge < 18 år.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-18 årErfaring savnes ved behandling af børn og unge under 18 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger begrænsede data.
Håndtering
Må ikke knuses.
Synkes hele.
Må ikke tygges.
Tages med et glas vand.
Kan tages med eller uden mad.
Depottabletternes hårde kerne kan udskilles i tabletlignende form med afføringen.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
Nedsat leverfunktion
- Forsigtighed ved let til moderat nedsat leverfunktion (Child-Pugh A og B). Dosisreduktion kan være nødvendigt pga. reduceret oral clearance.
- Erfaring savnes ved stærkt nedsat leverfunktion (Child-Pugh C og D).
Seponering
Angina pectoris: Gradvis nedtitrering af dosis skal overvejes for at undgå rebound-fænomen.
Kontraindikationer
- Svær hypotension
- Akut myokardieinfarkt (< 4 uger)
- Kardiovaskulært shock
- Ustabil angina pectoris
- Svær overfølsomhed for andre calciumantagonister
- Samtidig anvendelse af rifampicin
- Kocks reservoir (ileostomi efter proktokolektomi).
Forsigtighedsregler
- Svær aortastenose
- Hypotension med systolisk blodtryk < 90 mmHG.
- Tidligere alvorlig gastro-intestinal forsnævring pga. uopløselig matriks.
- Ved angina pectoris skal gradvis nedtitrering af dosis overvejes for at undgå rebound-fænomen.
- Calciumantagonister bør anvendes med forsigtighed ved svær hjerteinsufficiens (NYHA-klasse III og IV) eller ved hæmodynamisk ustabil hjerteinsufficiens efter akut myokardieinfarkt pga. den negative inotrope og perifer vasodilaterende effekt, hvor der er øget risiko for lungeødem. Calciumantagonister har ikke direkte rolle i behandling af hjerteinsufficiens, men studier viser, at det er sikkert at anvende amlodipin ved hjerteinsufficiens, hvor behandling med en calciumantagonist er indiceret.
- Natriumindhold
Adalat Oros 20 mg, depottabletter: 1 depottablet 20 mg indeholder 0,4 mmol natrium, som svarer til 21,2 mg natriumchlorid.
Adalat Oros 30 mg, depottabletter: 1 depottablet 30 mg indeholder 0,4 mmol natrium, som svarer til 23,9 mg natriumchlorid.
Adalat Oros 60 mg, depottabletter: 1 depottablet 60 mg indeholder 0,8 mmol natrium, som svarer til 47,8 mg natriumchlorid
Bivirkninger
Bivirkningerne er som regel milde, forbigående og dosisafhængige.
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Obstipation | |
| Almene symptomer og reaktioner på administrationsstedet | Utilpashed | |
| Nervesystemet | Hovedpine | |
| Vaskulære sygdomme | Ødemer | Vasodilatation |
| Ikke almindelige (0,1-1 %) | ||
| Hjerte | Palpitationer, Takykardi | |
| Øjne | Synsforstyrrelser | |
| Mave-tarm-kanalen | Abdominalsmerter | Dyspepsi, Flatulens, Kvalme, Mundtørhed |
| Almene symptomer og reaktioner på administrationsstedet | Smerter | Kuldefornemmelse |
| Immunsystemet | Allergiske reaktioner, Angioødem | |
| Undersøgelser | Forhøjede levertransaminaser | |
| Knogler, led, muskler og bindevæv | Muskelkramper | Hævede led |
| Nervesystemet | Migræne, Svimmelhed, Tremor | |
| Psykiske forstyrrelser | Angst | Søvnforstyrrelser |
| Nyrer og urinveje | Dysuri, Polyuri | |
| Det reproduktive system og mammae | Erektil dysfunktion | |
| Luftveje, thorax og mediastinum | Epistaxis, Nasal tilstopning | |
| Hud og subkutane væv | Erytem | |
| Vaskulære sygdomme | Hypotension, Synkope | |
| Sjældne (0,01-0,1 %) | ||
| Mave-tarm-kanalen | Gingival hyperplasi | |
| Immunsystemet | Urticaria | |
| Nervesystemet | Dysæstesi, Paræstesier | |
| Hud og subkutane væv | Hudkløe, Hududslæt | |
| Ikke kendt hyppighed | ||
| Blod og lymfesystem | Agranulocytose | |
| Hjerte | Angina pectoris | |
| Øjne | Øjensmerter | |
| Immunsystemet | Anafylaktisk reaktion | |
| Metabolisme og ernæring | Hyperglykæmi | |
| Knogler, led, muskler og bindevæv | Artralgi | Myalgi |
| Luftveje, thorax og mediastinum | Lungeødem (anvendt tokolytisk under graviditet) | |
| Hud og subkutane væv | Fotosensibilitet, Purpura, Toksisk epidermal nekrolyse (TEN) | |
Ved pludseligt ophør med behandlingen er der set øget frekvens eller forværring af angina, myokardieinfarkt, hjerteinsufficiens og ortostatisk hypotension.
Kliniske aspekter
Reflekstakykardi er hyppig, men problemet er reduceret med de registrerede depotformuleringer.
Obstipation, mavesmerter.
Interaktioner
- Kombinationen af andre antihypertensiva og nifedipin virker synergistisk. Ved samtidig indgift bør doseringen af nifedipin være forsigtig under kontrol af blodtryk og hjertefrekvens.
- Nifedipin metaboliseres via CYP3A4, og der er mulige interaktioner med inhibitorer og induktorer.
- Inhibitorer af CYP3A4, fx itraconazol, ketoconazol, voriconazol, erythromycin, fluoxetin og HIV-proteasehæmmere øger plasmakoncentrationen af nifedipin, og dosisreduktion af nifedipin kan være nødvendigt.
- Samtidig indtagelse af nifedipin og større mængder (herunder som juice) af grapefrugt eller pomelo kan øge AUC af nifedipin med op til en faktor 2, og indtag af større mængder (herunder som juice) af grapefrugt eller pomelo bør undgås.
- Rifampicin er en kraftig induktor af CYP3A4, og samtidig behandling med nifedipin indgift bør undgås, da rifampicin markant reducerer nifedipins biotilgængelighed og effekt.
- Andre induktorer, fx carbamazepin, phenytoin og naturlægemidler, som indeholder perikon, kan tilsvarende nedsætte plasmakoncentrationen af nifedipin.
- Forsigtighed ved samtidig administration af tacrolimus.
- Nøje overvågning af blodtrykket ved samtidig administration af intravenøst magnesiumsulfat pga. risiko for udtalt blodtryksfald, som kan skade både mor og barn.
- Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
Graviditet
Baggrund: Der er data for ca. 300 1. trimester-eksponerede uden tegn på overhyppighed af misdannelser. Datamængden tillader ikke at udelukke en øget risiko. Ved anvendelse i 2. og 3. trimester er datamængden begrænset. Tabletter kan dog anvendes ved truende for tidlig fødsel og som antihypertensivum ved præeklampsi. Se endvidere Hypertension hos gravide.
Ifølge Produktresumeet er akut lungeødem beskrevet, når calciumblokkere, herunder nifedipin, er blevet anvendt som tokolytisk lægemiddel under graviditet, især ved multiple graviditeter (tvillinger eller flere fostre), ved i.v. brug og/eller sammen med beta-2-agonister.
Se også: Klassifikation - graviditet
Amning
Baggrund: Den relative vægtjusterede dosis er ca. 2 %. Der er ikke beskrevet bivirkninger hos barnet.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Forsigtighed ved indtag af alkohol under behandling med Adalat® Oros.
Reaktionsevnen nedsættes.
Forgiftning
Farmakodynamik
Farmakokinetik
- Biotilgængelighed ca. 50 % pga. udtalt first pass-metabolisme i leveren.
- Maksimal plasmakoncentration efter 6-12 timer. Ved gentagen indgift opnås relativt konstant plasmakoncentration over et 24-timers doseringsinterval.
- Metaboliseres via CYP3A4 til inaktive metabolitter.
- Terminal plasmahalveringstid efter sidste dosis 2-4 timer.
- Depottabletter (monodepot) frigiver det aktive stof over 24 timer.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Depottabletter | 30 mg |
Farve
Andre
|
|
| 30 mg (Epione) |
Farve
Andre
|
||
| 30 mg (Orifarm) |
Farve
Andre
|
||
| 30 mg (Paranova) |
Farve
Andre
|
||
| 30 mg (Abacus) |
Farve
Andre
|
Firma
Tilskud
Klausuleret tilskud ved behandlingskrævende hypertension eller anden form for hjerte-kar-sygdom, hvor behandling med dihydropyridin-calciumantagonister med generelt tilskud uden klausulering ikke tolereres, eller i helt særlige tilfælde - efter lægens samlede kliniske vurdering af patientens tilstand - ikke er hensigtsmæssig.
For de patienter, der opfylder klausulen, påtegnes recepten med ordet "tilskud".
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | depottabletter
30 mg
(kan dosisdisp.)
Adalat Oros |
059803 |
98 stk. (blister)
|
197,95 | 2,02 | 2,02 | |
| (B) | depottabletter
30 mg
(Epione)
(kan dosisdisp.)
Adalat Oros |
425886 |
28 stk. (blister)
|
109,60 | 3,91 | 3,91 | |
| (B) | depottabletter
30 mg
(Epione)
(kan dosisdisp.)
Adalat Oros |
444708 |
98 stk. (blister)
|
252,30 | 2,57 | 2,57 | |
| (B) | depottabletter
30 mg
(Orifarm)
(kan dosisdisp.)
Adalat Oros |
376747 |
98 stk. (blister)
|
248,00 | 2,53 | 2,53 | |
| (B) | depottabletter
30 mg
(Paranova)
(kan dosisdisp.)
Adalat Oros |
115467 |
28 stk. (blister)
|
118,95 | 4,25 | 4,25 | |
| (B) | depottabletter
30 mg
(Abacus)
(kan dosisdisp.)
Adalat Oros |
182892 |
98 stk. (blister)
|
267,85 | 2,73 | 2,73 |
Substitution
| depottabletter 30 mg |
|---|
| Adalat LA (Parallelimport), Nifedipin, depottabletter 30 mg Genordn. B |
| Nifedipin "Paranova" (Parallelimport), Nifedipin, depottabletter 30 mg |
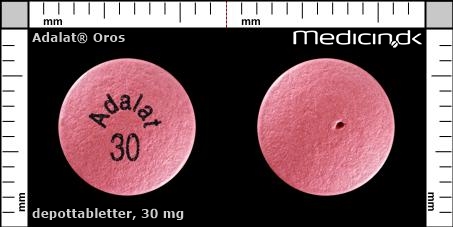
Foto og identifikation
Depottabletter 30 mg |
| Præg: |
Adalat, 30
|
| Kærv: | Ingen kærv |
| Farve: | Rosa |
| Mål i mm: | 9,1 x 9,1 |
Referencer
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
3878. Briggs GG, Freeman RK, Towers CV et al. Briggs: Drugs in Pregnancy and Lactation. Wolters Kluwer. 2021; 12th Edition, https://www.wolterskluwer.com/en/solutions/ovid/briggs-drugs-in-pregnancy-and-lactation-a-reference-guide-to-fetal-and-neonatal-risk-730 (Lokaliseret 19. marts 2026)
4039. Weber-Schoendorfer C, Hannemann D, Meister R et al. The safety of calcium channel blockers during pregnancy: a prospective, multicenter, observational study. Reprod Toxicol. 2008; 26(1):24-30, https://pubmed.ncbi.nlm.nih.gov/18585452/ (Lokaliseret 22. marts 2026)
4040. Magee LA, Schick B, Donnenfeld AE. The safety of calcium channel blockers in human pregnancy: a prospective, multicenter cohort study. Am J Obstet Gynecol. 1996; 174(3):823-8, https://pubmed.ncbi.nlm.nih.gov/8633650/ (Lokaliseret 22. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



