Yderligere information
Anvendelsesområder
Dispenseringsform
Vagitorier. 1 vagitorie indeholder 500 mg metronidazol.
Doseringsforslag
1 vagitorie (500 mg) placeres dybt i skeden 1 gang dgl. ved sengetid i 6 dage.
Bemærk:
- Erfaring savnes vedr. behandling af børn < 18 år.
- Seksuelt samkvem frarådes under infektionen og under behandling med vagitorier.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-18 årForsigtighed ved behandling af børn og unge under 18 år. Ingen yderligere oplysninger i produktresumé.
Instruktioner og anden information
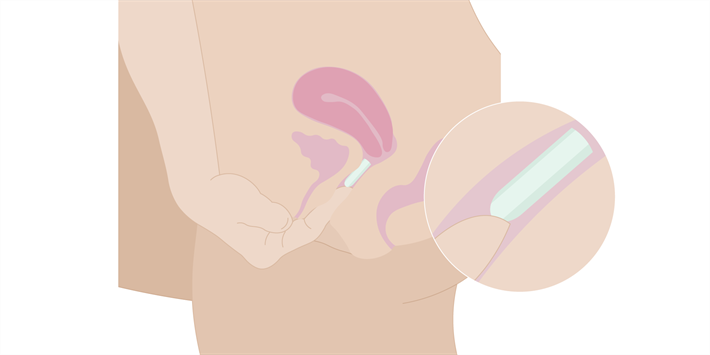
- Vask altid hænder før og efter indføring af vagitoriet.
- Vagitoriet indføres i skeden før sengetid. Placér det mellem kønslæberne, og pres det opad og bagud ind i skeden.
Bemærk:
- Fugt evt. vagitoriet med lidt vand for nemmere indføring.
- Det kan være nemmere at gøre, hvis du ligger ned eller sidder på hug.
- Vagitoriet skal ikke vende en bestemt vej.
Kontraindikationer
Forsigtighedsregler
Forsigtighed hos patienter med Cockaynes syndrom, da der er rapporteret tilfælde af svær hepatotoksicitet/akut leversvigt (herunder tilfælde med dødeligt udfald og meget hurtig symptomdebut) efter systemisk behandling med metronidazol.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Gastro-intestinale gener | |
| Almene symptomer og reaktioner på administrationsstedet | Træthed | |
| Metabolisme og ernæring | Hypofagi | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Psykiske forstyrrelser | Irritabilitet | |
| Det reproduktive system og mammae | Irritation og udflåd, Vaginal candidiasis, Vaginal kløe | |
| Ikke almindelige (0,1-1 %) | ||
| Mave-tarm-kanalen | Diarré, Flatulens, Kvalme, Mundtørhed, Smagsforstyrrelser | |
| Nervesystemet | Paræstesier | |
| Psykiske forstyrrelser | Depression | Søvnforstyrrelser |
| Nyrer og urinveje | Urinvejssymptomer | Misfarvning af urinen |
| Det reproduktive system og mammae | Gennembrudsblødning, Menstruationsforstyrrelser | |
| Hud og subkutane væv | Hudirritation, Tør hud | |
| Ikke kendt hyppighed | ||
| Immunsystemet | Hypersensitivitetsreaktioner*, Stevens-Johnsons syndrom* | Urticaria |
| Hud og subkutane væv | Akut generaliseret eksantematøs pustulose (AGEP)*, Toksisk epidermal nekrolyse (TEN)* | |
*Der er rapporteret tilfælde af svære bulløse hudreaktioner ved systemisk brug af metronidazol.
- Indeholder methylparahydroxybenzoat og propylparahydroxybenzoat, som kan medføre allergiske reaktioner (muligvis forsinkede) samt propylenglycol, som kan medføre hudirritation.
Kliniske aspekter
Lokale bivirkninger (irritation, kløe og udflåd, udvikling af candidiasis infektion) er de mest almindelige. Den systemiske absorption er lav, men gastrointestinale symptomer (fx kvalme og metalsmag) forekommer hos 5-10%.
Graviditet
Baggrund: Den systemiske absorption er ringe. For systemisk behandling med metronidazol er data for mange tusinde 1. trimester-eksponerede uden tegn på overhyppighed af uønsket fosterpåvirkning.
Se også: Klassifikation - graviditet
Amning
Baggrund: Den systemiske absorption er ringe.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol skal undgås under, samt 3 dage efter endt behandling med Flagyl®.
Patienten kan opleve en reaktion med opkastning, rødme i ansigtet og varmefølelse, hurtig vejrtrækning og hjertebanken.
Farmakodynamik
Virkemåde, virkningsspektrum og resistensforhold, se Metronidazol (systemisk brug).
Farmakokinetik
Den systemiske absorption er ringe. Se endvidere Metronidazol (systemisk brug).
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Vagitorier | 500 mg (Orifarm) |
Andre
|
|
| 500 mg (2care4) |
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | vagitorier
500 mg
(Orifarm)
Flagyl |
494485 |
10 stk. (blister)
|
373,70 | 37,37 | 37,37 | |
| (B) | vagitorier
500 mg
(2care4)
Flagyl |
564710 |
10 stk. (blister)
|
374,35 | 37,44 | 37,44 |
Referencer
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
4873. Sheehy O, Santos F, Ferreira E et al. The use of metronidazole during pregnancy: a review of evidence. Curr Drug Saf. 2015; 10(2):170-9, https://pubmed.ncbi.nlm.nih.gov/25986038/ (Lokaliseret 25. marts 2026)
3738. Koss CA, Baras DC, Lane SD et al. Investigation of metronidazole use during pregnancy and adverse birth outcomes. Antimicrob Agents Chemother. 2012; 56(9):4800-5, https://pubmed.ncbi.nlm.nih.gov/22751543/ (Lokaliseret 18. marts 2026)
152. Diav-Citrin O, Shechtman S, Gotteiner T et al. Pregnancy outcome after gestational exposure to metronidazole: a prospective controlled cohort study. Teratology. 2001; 63(5):186-92, https://pubmed.ncbi.nlm.nih.gov/11320529/ (Lokaliseret 18. marts 2026)
3737. Czeizel AE, Rockenbauer M. A population based case-control teratologic study of oral metronidazole treatment during pregnancy. Br J Obstet Gynaecol. 1998; 105(3):322-7, https://pubmed.ncbi.nlm.nih.gov/9532994/ (Lokaliseret 18. marts 2026)
3736. Piper JM, Mitchel EF, Ray WA. Prenatal use of metronidazole and birth defects: no association. Obstet Gynecol. 1993; 82(3):348-52, https://pubmed.ncbi.nlm.nih.gov/8355932/ (Lokaliseret 18. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



