Yderligere information
Antihypertensivum. Angiotensin II-receptorantagonist.
Anvendelsesområder
- Arteriel hypertension.
- Hjerteinsufficiens med nedsat systolisk venstre ventrikelfunktion (HFrEF) og/eller kliniske tegn på hjertesvigt efter AMI.
Andre anvendelsesområder
Dispenseringsform
Tabletter. 1 tablet indeholder 4 mg (delekærv), 8 mg (delekærv), 16 mg (delekærv) eller 32 mg (delekærv) candesartancilexetil.
Doseringsforslag
Hypertension
Voksne
- 8 mg 1 gang dgl.
- Dosis kan øges til 16 mg 1 gang dgl., maksimalt 32 mg dgl.
Børn > 6 år og unge < 18 år
- 4 mg 1 gang dgl.
- Dosis kan øges til:
- Vægt < 50 kg: maksimalt 8 mg 1 gang dgl.
- Vægt ≥ 50 kg: 8 mg 1 gang dgl., maksimalt 16 mg 1 gang dgl.
Hjerteinsufficiens
Voksne
- Initialt. 4 mg 1 gang dgl.
- Dosis kan fordobles med 2 ugers interval til maksimalt 32 mg dgl.
Bemærk:
- Sikkerhed og virkning hos børn i alderen 1 til < 6 år er ikke undersøgt. Se evt. data i Produktresume.
- Må ikke anvendes til børn < 1 år.
Børn og unge
-
Kontraindiceret
0-1 årMå ikke anvendes til børn under 1 år.
-
Forsigtighed, ingen eller begrænset erfaring
1-6 årErfaring savnes ved behandling af børn mellem 1 og 6 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger begrænsede data.
Håndtering
Kan knuses.
Synkes hele eller halve.
Knust tablet kan opslæmmes i vand.
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på kold, blød mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
forsigtighed, monitorering |
|
|---|---|
| GFR | Advarsel |
| <30 ml/min. |
|
Nedsat leverfunktion
Voksne
- Initialt 4 mg 1 gang dgl.
- Kontraindiceret ved stærkt nedsat leverfunktion og/eller kolestase.
Kontraindikationer
- Tidligere angioneurotisk ødem under behandling med angiotensin II-receptorantagonist (ARB).
- Samtidig behandling med aliskiren hos patienter med diabetes eller nedsat nyrefunktion (GFR < 60 ml/min).
Forsigtighedsregler
- Angioødem i anamnesen
- Nyrearteriestenose
- Mitralklapstenose
- Aortastenose
- Hypertrofisk kardiomyopati
- I forbindelse med de første doser er der hos enkelte patienter konstateret excessivt blodtryksfald, specielt ved samtidig behandling med diuretika og/eller andre vasodilatorer.
- Hypovolæmi bør korrigeres, før behandlingen indledes.
- Risiko for hyperkaliæmi ved samtidig indgift af aldosteronantagonister eller ACE-hæmmere.
- Studier har vist lavere antihypertensiv virkning hos afro-amerikanske patienter (sandsynligvis pga. generelt lavere plasma renin aktivitet). Risiko for lignende effekt hos andre patienter af afrikansk oprindelse.
- Der er indberettet intestinalt angioødem, med symptomer som mavesmerter, kvalme, opkastning og diarré der forsvandt efter seponering af angiotensin II-receptorantagonist (ARB).
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Infektioner og parasitære sygdomme | Luftvejsinfektion | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Vaskulære sygdomme | Hypotension | |
| Meget sjældne (< 0,01 %) | ||
| Blod og lymfesystem | Agranulocytose, Leukopeni | |
| Mave-tarm-kanalen | Kvalme | |
| Lever og galdeveje | Hepatitis | |
| Immunsystemet | Angioødem, Intestinalt angioødem | Urticaria |
| Undersøgelser | Forhøjede leverenzymer | |
| Metabolisme og ernæring | Hyperkaliæmi, Hyponatriæmi | |
| Knogler, led, muskler og bindevæv | Artralgi, Rygsmerter | Myalgi |
| Nyrer og urinveje | Kronisk nyresygdom, Nyrefunktionspåvirkning | |
| Luftveje, thorax og mediastinum | Hoste | |
| Hud og subkutane væv | Hudkløe, Hududslæt | |
| Ikke kendt hyppighed | ||
| Mave-tarm-kanalen | Diarré | |
- Hovedpine, svimmelhed, luftvejsinfektion og hoste forekommer meget almindeligt hos børn. Hududslæt almindeligt.
- Hyperkaliæmi, hyponatriæmi og leverpåvirkning er ikke almindeligt hos børn.
- Svimmelhed og hovedpine er almindelige ved behandling af hypertension, men meget sjældne ved behandling af hjerteinsufficiens.
- Hyperkaliæmi og nedsat nyrefunktion er meget sjældne ved behandling af hypertension, men almindelige ved behandling af hjerteinsufficiens.
Kliniske aspekter
- Risiko for udtalt blodtryksfald er registreret hos patienter med stærkt aktiveret renin-angiotensin-aldosteron system, især i starten af behandling med kombinationsbehandling. Lavere startdosis kan anvendes.
- I tilfælde af angioneurotisk ødem (meget sjældent), er skift til anden angiotensin II-antagonist eller ACE-hæmmer kontraindiceret.
- Svimmelhed, hovedpine samt ortostatisk hypotension er oftest forbigående.
Interaktioner
- Kalium, kaliumbesparende diuretika og andre lægemidler (fx heparin, trimetoprim/sulfametoxazol), som øger serum-kalium kan forårsage hyperkaliæmi.
- Lithiumkoncentrationen kan øges, hvorfor kontrol af serum-lithiumniveau anbefales.
- NSAID kan svække den antihypertensive effekt.
- Samtidig behandling med aliskiren hos patienter med diabetes eller nedsat nyrefunktion (GFR < 60 ml/min) kan give kraftige bivirkninger og er kontraindiceret.
- Samtidig anvendelse af ACE-hæmmere eller aliskiren (dobbelthæmning af renin-angiotensin-aldosteronsystemet) øger risikoen for hypotension, hyperkaliæmi og nedsat nyrefunktion (inklusiv akut nyresvigt). Kombinationen frarådes.
Graviditet
Baggrund: Der er meget sparsomme data for angiotensin II-antagonister med lidt over 300 gravide eksponeret i 1. trimester af graviditeten. Der er beskrevet oligohydramnios, anuri, væksthæmning og neonatal hypotension, specielt ved eksponering i 2. og 3. trimester.
Der er ikke specifikke data for candesartan, som tillader et meningsfyldt risikoestimat.
Se endvidere Hypertension hos gravide.
Se også: Klassifikation - graviditet
Amning
Baggrund: RVD er 0,1 % baseret på data fra 3 ammende kvinder. Plasmakoncentrationen er målt på 2 børn og var i begge tilfælde under detektionsgrænsen.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Candemox® påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
- Blokerer angiotensin-II-type 1-receptoren, hvilket resulterer i en forhøjelse af plasma-renin- og angiotensin-II-niveauerne samt nedsat aldosteron i plasma. Den kliniske effekt er universel vasodilatation uden sympatikusaktivering som ved ACE-hæmmere.
- Virkningen indtræder inden for 2 timer. Virkningsvarighed ca. 24 timer.
Farmakokinetik
- Candesartancilexetil er en prodrug, som i tarmvæggen hydrolyseres til den aktive substans candesartan.
- Biotilgængelighed ca. 15 %.
- Maksimal plasmakoncentration efter ca. 4 timer.
- Plasmahalveringstid 9-12 timer.
- Ca. 25 % udskilles gennem nyrerne i form af candesartan.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Tabletter | 4 mg |
Andre
|
|
| 8 mg |
Farve
Andre
|
||
| 16 mg |
Farve
Andre
|
||
| 32 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | tabletter
4 mg
(kan dosisdisp.)
Candemox |
435278 |
100 stk. (blister)
|
94,85 | 0,95 | 1,90 | |
| (B) | tabletter
4 mg
(kan dosisdisp.)
Candemox |
040458 |
120 stk.
|
Udgået 10-11-2025 | |||
| (B) | tabletter
8 mg
(kan dosisdisp.)
Candemox |
599317 |
100 stk. (blister)
|
54,10 | 0,54 | 0,54 | |
| (B) | tabletter
16 mg
(kan dosisdisp.)
Candemox |
105305 |
30 stk. (blister)
|
190,10 | 6,34 | 3,17 | |
| (B) | tabletter
16 mg
(kan dosisdisp.)
Candemox |
568991 |
100 stk. (blister)
|
43,55 | 0,44 | 0,22 | |
| (B) | tabletter
16 mg
(kan dosisdisp.)
Candemox |
373553 |
120 stk.
|
Udgået 19-01-2026 | |||
| (B) | tabletter
32 mg
(kan dosisdisp.)
Candemox |
483557 |
100 stk. (blister)
|
61,85 | 0,62 | 0,15 |
Substitution
| tabletter 4 mg |
|---|
| Candesartan "Krka" KRKA, Candesartancilexetil, tabletter 4 mg Genordn. B |
| Candesartan "Medical Valley" Medical Valley, Candesartancilexetil, tabletter 4 mg |
| Candesartan "Orion" Orion Pharma, Candesartancilexetil, tabletter 4 mg Genordn. B |
| Candesartan "Stada" STADA Nordic, Candesartancilexetil, tabletter 4 mg Genordn. B |
| tabletter 8 mg |
|---|
| Atacand Cheplapharm, Candesartancilexetil, tabletter 8 mg Genordn. B |
| Candesartan "Krka" KRKA, Candesartancilexetil, tabletter 8 mg Genordn. B |
| Candesartan "Medical Valley" Medical Valley, Candesartancilexetil, tabletter 8 mg |
| Candesartan "Orion" Orion Pharma, Candesartancilexetil, tabletter 8 mg Genordn. B |
| Candesartan "Stada" STADA Nordic, Candesartancilexetil, tabletter 8 mg Genordn. B |
| Kairasec Medical Valley, Candesartancilexetil, tabletter 8 mg Genordn. B |
| Kandrozid Viatris, Candesartancilexetil, tabletter 8 mg Genordn. B |
| tabletter 16 mg |
|---|
| Atacand Cheplapharm, Candesartancilexetil, tabletter 16 mg Genordn. B |
| Candesartan "Krka" KRKA, Candesartancilexetil, tabletter 16 mg Genordn. B |
| Candesartan "Medical Valley" Medical Valley, Candesartancilexetil, tabletter 16 mg |
| Candesartan "Orion" Orion Pharma, Candesartancilexetil, tabletter 16 mg Genordn. B |
| Candesartan "Stada" STADA Nordic, Candesartancilexetil, tabletter 16 mg Genordn. B |
| Kairasec Medical Valley, Candesartancilexetil, tabletter 16 mg Genordn. B |
| Kandrozid Viatris, Candesartancilexetil, tabletter 16 mg Genordn. B |
| tabletter 32 mg |
|---|
| Candesartan "Epione Medicine" (Parallelimport), Candesartancilexetil, tabletter 32 mg Genordn. B |
| Candesartan "Krka" KRKA, Candesartancilexetil, tabletter 32 mg Genordn. B |
| Candesartan "Medical Valley" Medical Valley, Candesartancilexetil, tabletter 32 mg |
| Candesartan "Orion" Orion Pharma, Candesartancilexetil, tabletter 32 mg Genordn. B |
| Candesartan "Stada" STADA Nordic, Candesartancilexetil, tabletter 32 mg Genordn. B |
| Kairasec Medical Valley, Candesartancilexetil, tabletter 32 mg Genordn. B |
Foto og identifikation
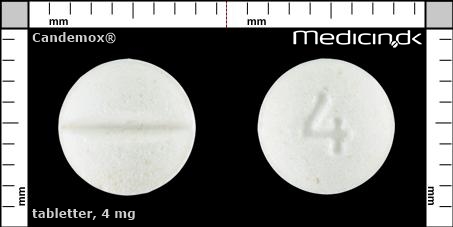
Tabletter 4 mg |
| Præg: |
4
|
| Kærv: | Delekærv |
| Farve: | Hvid |
| Mål i mm: | 6,6 x 6,6 |
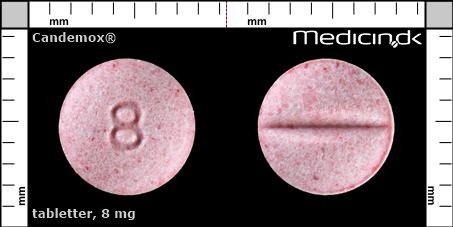
Tabletter 8 mg |
| Præg: |
8
|
| Kærv: | Delekærv |
| Farve: | Lyserød, Spættet |
| Mål i mm: | 6,5 x 6,5 |
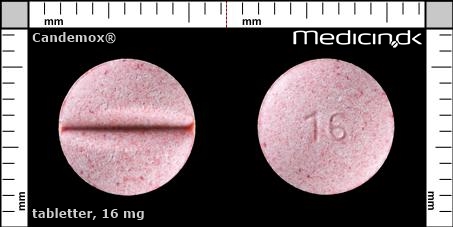
Tabletter 16 mg |
| Præg: |
16
|
| Kærv: | Delekærv |
| Farve: | Lyserød, Spættet |
| Mål i mm: | 8,6 x 8,6 |
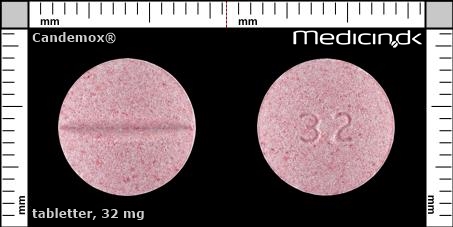
Tabletter 32 mg |
| Præg: |
32
|
| Kærv: | Delekærv |
| Farve: | Lyserød, Spættet |
| Mål i mm: | 11,4 x 11,4 |
Referencer
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
5754. Coberger ED, Jensen BP, Dalrymple JM. Transfer of Candesartan Into Human Breast Milk. Obstet Gynecol. 2019; 134(3):481-4, https://pubmed.ncbi.nlm.nih.gov/31403599/ (Lokaliseret 25. marts 2026)
4332. Shimada C, Akaishi R, Cho K et al. Outcomes of 83 fetuses exposed to angiotensin receptor blockers during the second or third trimesters: a literature review. Hypertens Res. 2015; 38(5):308-13, https://pubmed.ncbi.nlm.nih.gov/25693853/ (Lokaliseret 25. marts 2026)
4329. Walfisch A, Al-maawali A, Moretti ME et al. Teratogenicity of angiotensin converting enzyme inhibitors or receptor blockers. J Obstet Gynaecol. 2011; 31(6):465-72, https://pubmed.ncbi.nlm.nih.gov/21823839/ (Lokaliseret 25. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



