Yderligere information
Antiviralt middel. Hæmmer det HIV-specifikke enzym reverse transcriptase.
Anvendelsesområder
Anvendes i kombination med andre antiretrovirale lægemidler til HIV-inficerede voksne og børn. Se endvidere kombinationsbehandling i Midler mod HIV.
Lamivudin bør kun anvendes, når behandlingen forestås af læger med særlig indsigt i HIV-associerede sygdomme og deres behandling.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 150 mg (delekærv) eller 300 mg lamivudin.
Doseringsforslag
- Voksne og børn med legemsvægt ≥ 25 kg
- 150 mg 2 gange dgl. eller 300 mg 1 gang dgl.
- Børn > 3 mdr. og med legemsvægt < 25 kg
Bemærk:
- Tidsinterval mellem doser ved skift mellem 1 dosis og 2 doser i døgnet:
- Fra 2 doser til 1 dosis: Ca. 12 timer
- Fra 1 dosis til 2 doser: Ca. 24 timer.
- Tabletter bør så vidt muligt anvendes til børn, da børn behandlet med oral opløsning kan udvikle hyppigere viral resistens end børn behandlet med tabletter.
- Erfaring savnes vedr. børn < 3 måneder.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-3 månederErfaring savnes ved behandling af børn under 3 måneder. De begrænsede data, der foreligger, er utilstrækkelige til at foreslå specifikke doseringsanbefalinger.
Håndtering
Kan knuses.
Bemærk: Knusning kan nedsætte/øge virkningen af tabletterne, og derfor er ekstra kontrol nødvendigt.
Knust tablet kan opslæmmes i vand.
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på en skefuld kold, blød mad, fx yoghurt eller æblemos.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
forsigtighed, dosisjustering |
|||
|---|---|---|---|
| GFR | Alder | Vægt | Advarsel |
| <5 ml/min. | 2-17 år | <25 KG |
HIV: Initialdosis 1,6 mg pr. kg, derefter vedligeholdelsesdosis på højst 0,9 mg pr. kg legemsvægt dgl. |
| ≥6 år | ≥25 KG |
HIV: Initialdosis 50 mg, derefter vedligeholdelsesdosis på højst 25 mg 1 gang dgl. |
|
| 5-15 ml/min. | 2-17 år | <25 KG |
HIV: Initialdosis 5 mg pr. kg, derefter vedligeholdelsesdosis på højst 1,6 mg pr. kg legemsvægt dgl. |
| ≥6 år | ≥25 KG |
HIV: Initialdosis 150 mg, derefter vedligeholdelsesdosis på højst 50 mg 1 gang dgl. |
|
| 15-30 ml/min. | 2-17 år | <25 KG |
HIV: Initialdosis 5 mg pr. kg, derefter vedligeholdelsesdosis på højst 3,3 mg pr. kg legemsvægt dgl. |
| ≥6 år | ≥25 KG |
HIV: Initialdosis 150 mg, derefter vedligeholdelsesdosis på højst 100 mg 1 gang dgl. |
|
| 30-50 ml/min. | 2-17 år | <25 KG |
HIV: Højst 5 mg pr. kg legemsvægt dgl. |
| ≥6 år | ≥25 KG |
HIV: Højst 150 mg 1 gang dgl. |
|
Nedsat leverfunktion
Forsigtighedsregler
Udvikles pancreatitis, bør lamivudin seponeres.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Kvalme, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Pyreksi, Træthed, Utilpashed | |
| Knogler, led, muskler og bindevæv | Artralgi | Myalgi |
| Nervesystemet | Hovedpine | |
| Psykiske forstyrrelser | Søvnløshed | |
| Luftveje, thorax og mediastinum | Hoste, Rhinitis | |
| Hud og subkutane væv | Alopeci | Hududslæt |
| Ikke almindelige (0,1-1 %) | ||
| Blod og lymfesystem | Anæmi, Neutropeni, Trombocytopeni | |
| Undersøgelser | Forhøjet ALAT | |
| Sjældne (0,01-0,1 %) | ||
| Mave-tarm-kanalen | Pancreatitis | |
| Lever og galdeveje | Hepatitis | |
| Immunsystemet | Angioødem | |
| Undersøgelser | Forhøjet plasma-amylase | |
| Knogler, led, muskler og bindevæv | Rhabdomyolyse | |
| Meget sjældne (< 0,01 %) | ||
| Blod og lymfesystem | Erytrocytaplasi | |
| Metabolisme og ernæring | Lactatacidose | |
| Nervesystemet | Perifer neuropati | |
Kliniske aspekter
- Bivirkningerne herover er opgjort på baggrund af studier, hvor der blev givet anden HIV-behandling samtidig. Det er derfor usikkert, i hvor høj grad bivirkningerne kan tilskrives lamivudin, som erfaringsmæssigt tåles godt.
- Hos HIV-inficerede patienter med svær immuninsufficiens kan der ved påbegyndelse af antiretroviral kombinationsbehandling opstå en inflammatorisk reaktion på asymptomatiske eller residuale opportunistiske infektioner. Autoimmune sygdomme (som fx. Graves´ sygdom og autoimmun hepatitis) er også blevet rapporteret i forbindelse med immunreaktivering; dog er den rapporterede tid til frembrud mere variabel, og frembrud kan forekomme mange måneder efter behandlingsstart.
- Særligt hos patienter med generelt anerkendte risikofaktorer, fremskreden HIV-sygdom eller langvarig kombinationsbehandling med antiretrovirale lægemidler er der rapporteret om tilfælde af osteonekrose. Hyppigheden heraf er ukendt.
- Legemsvægt og lipidkoncentration i blodet kan stige under antiretroviral kombinationsbehandling, se Midler mod HIV.
Interaktioner
- Samtidig indgift af lamivudin og trimethoprim øger plasmakoncentrationen af lamivudin. Dosisjustering kan være nødvendig.
- Vedvarende samtidig brug af sorbitolholdige lægemidler eller andre osmotisk virkende polyalkoholer, fx xylitol og mannitol, bør så vidt muligt undgås, fordi AUC og maksimal plasmakoncentration af lamivudin derved kan blive reduceret.
Graviditet
Baggrund: Store epidemiologiske studier viser samstemmende, at antiretroviral behandling under graviditeten (for alle lægemidler og kombinationer er der data for i alt > 35.000 gravide; heraf > 16.000 eksponeret i 1. trimester) ikke er forbundet med en overhyppighed af medfødte misdannelser. Visse studier viser en lidt øget risiko for tidlig fødsel og lav fødselsvægt, men det er uklart, om og i hvilket omfang dette kan tilskrives behandlingen.
For lamivudin er der data for over 5.500 1. trimester-eksponerede uden tegn på overhyppighed af uønsket fosterpåvirkning.
Behandling af gravide med HIV-infektion er en specialistopgave. Se endvidere Midler mod HIV.
Se også: Klassifikation - graviditet
Amning
Baggrund: Amning frarådes på grund af smitterisiko.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Forsigtighed ved indtagelse af alkohol under behandling med Lamivudin "Teva Pharma BV".
Alkoholforbrug kan bidrage til tilfælde af osteonekrose.
Farmakodynamik
- HIV-nukleosid-RT-hæmmer.
- Intracellulært omdannes det enzymatisk til den aktive metabolit, som hæmmer replikationen af virus.
Farmakokinetik
- Biotilgængelighed ca. 80 %.
- Maksimal plasmakoncentration efter ca. 1 time.
- Plasmahalveringstid 5-7 timer.
- Ca. 70 % udskilles uomdannet gennem nyrerne.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Filmovertrukne tabletter | 150 mg |
Farve
Andre
|
|
| 300 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (BEGR) | filmovertrukne tabletter
150 mg
(kan dosisdisp.)
Lamivudin "Teva Pharma BV" |
537098 |
60 stk. (Orifarm)
|
1.319,90 | 22,00 | 44,00 | |
| (BEGR) | filmovertrukne tabletter
300 mg
(kan dosisdisp.)
Lamivudin "Teva Pharma BV" |
045554 |
30 stk. (blister)
|
600,70 | 20,02 | 20,02 |
Foto og identifikation
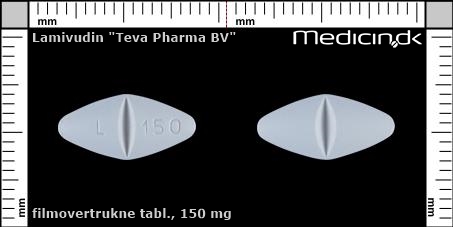
Filmovertrukne tabletter 150 mg |
| Præg: |
L 150
|
| Kærv: | Delekærv |
| Farve: | Lysegrå |
| Mål i mm: | 7 x 14,5 |
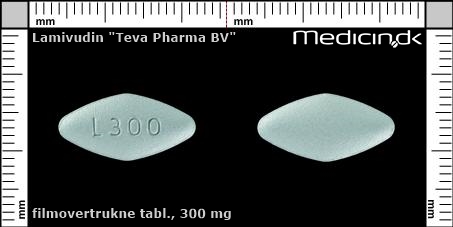
Filmovertrukne tabletter 300 mg |
| Præg: |
L 300
|
| Kærv: | Ingen kærv |
| Farve: | Grå |
| Mål i mm: | 8 x 18 |
Referencer
4375. Gandhi RT, Bedimo R, Hoy JF et al. Antiretroviral Drugs for Treatment and Prevention of HIV Infection in Adults: 2022 Recommendations of the International Antiviral Society-USA Panel. JAMA. 2023; 329-(1):63-84, https://pubmed.ncbi.nlm.nih.gov/33052386/ (Lokaliseret 25. marts 2026)
4376. European Pregnancy and Paediatric HIV Cohort Collaboration (EPPICC) Study Group. Nucleoside reverse transcriptase inhibitor backbones and pregnancy outcomes. AIDS. 2019; 33(2):295-304, https://pubmed.ncbi.nlm.nih.gov/30562172/ (Lokaliseret 25. marts 2026)
4377. Veroniki AA, Antony J, Straus SE et al. Comparative safety and effectiveness of perinatal antiretroviral therapies for HIV-infected women and their children: Systematic review and network meta-analysis including different study designs. PLoS One. 2018; 13(6), https://pubmed.ncbi.nlm.nih.gov/29912896/ (Lokaliseret 25. marts 2026)
4379. Rough K, Seage GR 3rd, Williams PL et al. Birth Outcomes for Pregnant Women with HIV Using Tenofovir-Emtricitabine. N Engl J Med. 2018; 378(17):1593-603, https://pubmed.ncbi.nlm.nih.gov/29694825/ (Lokaliseret 25. marts 2026)
4378. Zash R, Jacobson DL, Diseko M et al. Comparative Safety of Antiretroviral Treatment Regimens in Pregnancy. JAMA Pediatr. 2017; 171(10), https://pubmed.ncbi.nlm.nih.gov/28783807/ (Lokaliseret 25. marts 2026)
4374. Antiretroviral Pregnancy Registry Advisory Committee. Interim Report. ANTIRETROVIRAL PREGNANCY REGISTRY. 1989-2023, https://www.apregistry.com/InterimReport.aspx (Lokaliseret 25. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



