Selektiv IP-receptoragonist til behandling af pulmonal hypertension.
Anvendelsesområder
Langvarig behandling af pulmonal arteriel hypertension (PAH) hos voksne patienter i WHO-funktionsklasse II-III, enten
- som kombinationsbehandling hos patienter, der ikke opnår tilstrækkelig effekt med en endothelinreceptorantagonist (ERA) og/eller en phosphodiesterase type 5-hæmmer (PDE-5-hæmmer), eller
- som monoterapi hos patienter, der ikke er kandidater til disse behandlinger.
Bør kun anvendes, når behandlingen forestås af læger med særlig indsigt i behandling af PAH.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 200, 400, 600, 800, 1.000, 1.200 1.400 eller 1.600 mikrogram selexipag.
Doseringsforslag
Voksne
- Initialt 200 mikrogram 2 gange dgl. morgen og aften.
- Dosis øges med 200 mikrogram morgen og aften med ugentlige intervaller til maksimalt 1.600 mikrogram 2 gange dgl.
- Ved start af behandlingen og ved hvert optitreringstrin anbefales det, at første dosis tages om aftenen.
Clopidogrel, deferasirox og teriflunomid
- Ved samtidig behandling med moderate CYP2C8-hæmmere, som clopidogrel, deferasirox og teriflunomid, skal dosis reduceres til det halve ved at give halv dosis 2 gange dgl. Alternativt gives fuld dosis kun én gang dgl. Efter seponering af den moderate CYP2C8-hæmmer genoptages dosering 2 gange dgl.
Bemærk:
- Bør ikke anvendes til børn < 2 år.
- Begrænset erfaring vedr. børn og unge 2 år - 18 år. Tilgængelige data i produktresumé.
- Begrænset erfaring vedr. ældre > 75 år.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
2-18 årBegrænset erfaring ved behandling af børn og unge 2 år - 18 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger begrænsede data i produktresumé.
-
Forsigtighed, bør ikke anvendes, utilstrækkelige data
0-2 årErfaring savnes ved behandling af børn under 2 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger ingen data.
Glemt medicin
- Glemt dosis kan tages indtil 6 timer før næste fastlagte dosis.
- Hvis indtagelse af tabletterne er glemt i ≥ 3 dage, skal behandlingen med selexipag genoptages med en lavere dosis og efterfølgende optitrering.
Håndtering
Kan knuses.
Synkes hele med et glas vand.
Tablet eller knust tablet kan opslæmmes i vand.
Bør tages til et måltid.
Knust tablet kan kommes på kold, blød mad.
Tabletterne kan bedres tåles, når de tages i forbindelse med et måltid.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
forsigtighed, dosisjustering |
|
|---|---|
| GFR | Advarsel |
| <30 ml/min. |
Forsigtighed ved optitrering af dosis. Dialyse: Ingen erfaring. |
Nedsat leverfunktion
- Kontraindiceret ved stærkt nedsat leverfunktion (Child-Pugh C) pga. manglende erfaring.
- Ved moderat nedsat leverfunktion (Child-Pugh B) bør startdosis være 200 mikrogram én gang dgl. Dosis øges med ugentlige intervaller i trin af 200 mikrogram én gang dgl. indtil utålelige eller medicinsk uhåndterbare bivirkninger.
Kontraindikationer
- Svær koronarhjertesygdom eller ustabil angina.
- Myokardieinfarkt inden for de sidste 6 mdr.
- Dekompenseret hjertesvigt, hvis dette ikke er under tæt medicinsk overvågning.
- Svære arytmier.
- Cerebrovaskulære hændelser (fx transitorisk iskæmisk attak, slagtilfælde) inden for de sidste 3 mdr.
- Kongenitte eller erhvervede klapdefekter med klinisk relevante forstyrrelser i myokardiefunktionen, som ikke er relateret til pulmonal hypertension.
- Samtidig behandling med stærke CYP2C8-hæmmere, som gemfibrozil, kan øge eksponeringen af selexipag betydeligt, og samtidig behandling er kontraindiceret.
Forsigtighedsregler
- Blodtryksfald kan forekomme, især ved forudgående hypotension, hypovolæmi eller svær obstruktion i venstre ventrikels udløbsdel.
- Behandlingen kan medføre hypertyroidisme. Tyroideafunktionstest udføres efter klinisk behov.
- Ved pulmonal veno-okklusiv sygdom kan der opstå tegn på lungeødem.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Meget almindelige (> 10 %) | ||
| Mave-tarm-kanalen | Diarré, Kvalme, Opkastning | |
| Knogler, led, muskler og bindevæv | Artralgi, Smerter i ekstremiteter | Kæbesmerter, Myalgi |
| Nervesystemet | Hovedpine | |
| Luftveje, thorax og mediastinum | Nasopharyngitis | |
| Vaskulære sygdomme | Rødme og varmefølelse | |
| Almindelige (1-10 %) | ||
| Blod og lymfesystem | Anæmi | |
| Det endokrine system | Hypertyroidisme | |
| Mave-tarm-kanalen | Abdominalsmerter | Dyspepsi |
| Almene symptomer og reaktioner på administrationsstedet | Smerter | |
| Immunsystemet | Angioødem | Urticaria |
| Undersøgelser | Vægttab | |
| Metabolisme og ernæring | Hypofagi | |
| Luftveje, thorax og mediastinum | Nasal tilstopning | |
| Hud og subkutane væv | Erytem | Hududslæt |
| Vaskulære sygdomme | Hypotension | |
| Ikke almindelige (0,1-1 %) | ||
| Hjerte | Takykardi | |
Kliniske aspekter
- Hyppigste bivirkninger ved selexipag omfatter hovedpine, diarre og kvalme.
- Behandlingen optitreres gradvist til den maksimalt tolererede dosis som justeres individuelt efter bivirkningsprofil.
- Bivirkninger optræder karakteristisk i optitreringsfasen.
- Angioødem er blevet rapporteret efter markedsføring med en latenstid, der kan overstige 30 dages behandling.
Interaktioner
- Samtidig behandling med stærke CYP2C8-hæmmere, som gemfibrozil, kan øge eksponeringen af selexipag betydeligt, og samtidig behandling er kontraindiceret.
- Ved samtidig behandling med moderate CYP2C8-hæmmere, som clopidogrel, deferasirox og teriflunomid, skal dosis reduceres til halv doisis 2 gange dgl., alternativt fuld dosis én gang dgl. Efter seponering af den moderate CYP2C8-hæmmer genoptages dosis 2 gange dgl.
- Forsigtighed ved samtidig behandling med stærke UGT1A3- og UGT2B7-hæmmere, som probenecid, fluconazol og valproat, pga. mulige interaktioner.
- CYP2C8 -induktorer, som rifampicin og carbamazepin, kan mindske eksponeringen af den aktive metabolit, og dosisjustering af selexipag kan være nødvendigt.
- Selexipag i kombination med både en endothelinreceptorantagonist (ERA) og en PDE-5-hæmmer resulterede i 30 % lavere eksponering for den aktive metabolit.
Graviditet
Baggrund: Der er ingen humane data, som tillader et meningsfyldt risikoestimat.
Se også: Klassifikation - graviditet
Fertile kvinder og mænd
Kvinder i den fertile alder skal anvende sikker kontraception under behandlingen.
Amning
Baggrund: Der er ikke kvantitative data for udskillelse i modermælk.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Uptravi påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Forgiftning
Der iværksættes understøttende tiltag efter behov. Dialyse er sandsynligvis ikke nyttig, idet selexipag og dets aktive metabolit har høj proteinbinding.
Farmakodynamik
Selektiv IP-receptoragonist. Stimulation af IP-receptoren fører til vasodilatoriske og antiproliferative og antifibrotiske virkninger.
Farmakokinetik
- Absorberes hurtigt fra mave-tarm-kanalen.
- Biotilgængelighed ca. 49 % pga. first pass-metabolisme.
- Hydrolyseres af CES1 i leveren til en aktiv metabolit, som er ca. 37 gange mere potent end selexipag.
- Maksimal plasmakoncentration efter 1-3 timer (selexipag) og 3-4 timer (aktive metabolit).
- Fordelingsvolumen ca. 0,17 l/kg.
- Plasmahalveringstid 6-14 timer (aktive metabolit).
- Ca. 12 % udskilles gennem nyrerne, resten med fæces.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Filmovertrukne tabletter | 200 mikrogram |
Farve
Andre
|
|
| 400 mikrogram |
Farve
Andre
|
||
| 600 mikrogram |
Farve
Andre
|
||
| 800 mikrogram |
Farve
Andre
|
||
| 1000 mikrogram |
Farve
Andre
|
||
| 1200 mikrogram |
Farve
Andre
|
||
| 1400 mikrogram |
Farve
Andre
|
||
| 1600 mikrogram |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (BEGR) | filmovertrukne tabletter
200 mikrogram
(kan dosisdisp.)
Uptravi |
167682 |
60 stk. (blister)
|
31.723,00 | 528,72 | 4.758,21 | |
| (BEGR) | filmovertrukne tabletter
200 mikrogram
(kan dosisdisp.)
Uptravi |
374906 |
140 stk. (blister)
|
73.956,45 | 528,26 | 4.754,21 | |
| (BEGR) | filmovertrukne tabletter
400 mikrogram
(kan dosisdisp.)
Uptravi |
522752 |
60 stk. (blister)
|
31.723,00 | 528,72 | 2.379,28 | |
| (BEGR) | filmovertrukne tabletter
600 mikrogram
(kan dosisdisp.)
Uptravi |
409733 |
60 stk. (blister)
|
31.723,00 | 528,72 | 1.586,15 | |
| (BEGR) | filmovertrukne tabletter
800 mikrogram
(kan dosisdisp.)
Uptravi |
186073 |
60 stk. (blister)
|
31.723,00 | 528,72 | 1.189,60 | |
| (BEGR) | filmovertrukne tabletter
1000 mikrogram
(kan dosisdisp.)
Uptravi |
386892 |
60 stk. (blister)
|
31.723,00 | 528,72 | 951,70 | |
| (BEGR) | filmovertrukne tabletter
1200 mikrogram
(kan dosisdisp.)
Uptravi |
489081 |
60 stk. (blister)
|
31.723,00 | 528,72 | 793,08 | |
| (BEGR) | filmovertrukne tabletter
1400 mikrogram
(kan dosisdisp.)
Uptravi |
413671 |
60 stk. (blister)
|
31.723,00 | 528,72 | 679,77 | |
| (BEGR) | filmovertrukne tabletter
1600 mikrogram
(kan dosisdisp.)
Uptravi |
172595 |
60 stk. (blister)
|
31.723,00 | 528,72 | 594,81 |
Foto og identifikation
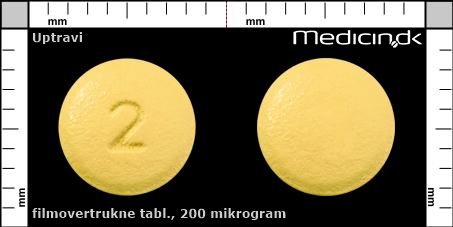
Filmovertrukne tabletter 200 mikrogram |
| Præg: |
2
|
| Kærv: | Ingen kærv |
| Farve: | Lysegul |
| Mål i mm: | 7 x 7 |
Filmovertrukne tabletter 400 mikrogram |
| Præg: |
4
|
| Kærv: | Ingen kærv |
| Farve: | Rødbrun |
| Mål i mm: | 7 x 7 |

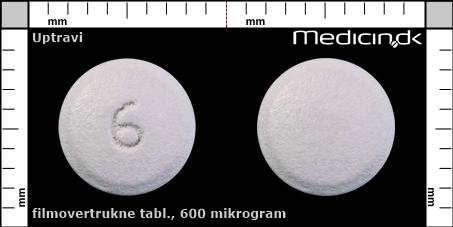
Filmovertrukne tabletter 600 mikrogram |
| Præg: |
6
|
| Kærv: | Ingen kærv |
| Farve: | Lys lilla |
| Mål i mm: | 7 x 7 |
Filmovertrukne tabletter 800 mikrogram |
| Præg: |
8
|
| Kærv: | Ingen kærv |
| Farve: | Mørkegrøn |
| Mål i mm: | 7 x 7 |

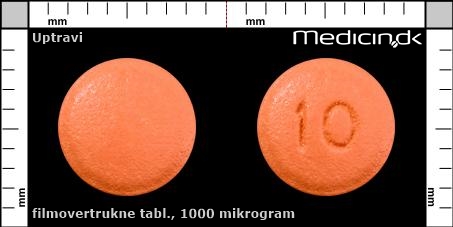
Filmovertrukne tabletter 1000 mikrogram |
| Præg: |
10
|
| Kærv: | Ingen kærv |
| Farve: | Orange |
| Mål i mm: | 7 x 7 |
Filmovertrukne tabletter 1200 mikrogram |
| Præg: |
12
|
| Kærv: | Ingen kærv |
| Farve: | Lilla |
| Mål i mm: | 7 x 7 |

Filmovertrukne tabletter 1400 mikrogram |
| Præg: |
14
|
| Kærv: | Ingen kærv |
| Farve: | Mørkegul |
| Mål i mm: | 7 x 7 |

Filmovertrukne tabletter 1600 mikrogram |
| Præg: |
16
|
| Kærv: | Ingen kærv |
| Farve: | Brun |
| Mål i mm: | 7 x 7 |

Referencer
1550. SPC, Lægemiddelstyrelsen. , https://www.produktresume.dk/AppBuilder/search (Lokaliseret 27. marts 2026)
3966. SPC, EMA. European Medicines Agency. , https://www.ema.europa.eu/en/medicines (Lokaliseret 19. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



