Yderligere information
Anvendelsesområder
Den antikonceptionelle sikkerhed er væsentlig mindre end ved de sædvanlige orale antikonceptionsmetoder.
Dispenseringsform
Tabletter. 1 tablet indeholder 1,5 mg levonorgestrel.
Doseringsforslag
Voksne og unge
1,5 mg hurtigst muligt efter coitus (helst inden for 12 timer og ikke senere end 72 timer).
Bemærk:
- Begrænsede data vedrørende anvendelse til kvinder < 16 år.
Børn og unge
-
Kontraindiceret, uegnet
0-13 årPræparatet er kun indiceret efter menarche.
Håndtering
Må ikke knuses.
Tages med et glas vand.
Kan tages med eller uden mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
Nedsat leverfunktion
Forsigtighedsregler
- Ved opkastning mindre end 3 timer efter tabletindtagelsen er metoden usikker, og man kan indtage en ny tablet.
- Bør højst anvendes én gang pr. cyklus på grund af risiko for bivirkninger.
- Ved mere end 5 dages forsinket menstruation eller ved unormal blødning bør graviditetstest udføres.
- Kvinder, der har behov for postcoital svangerskabsforebyggelse, og som har indtaget et enzyminducerende lægemiddel inden for de seneste 4 uger (se evt. interaktioner), rådes til at bruge et ikke-hormonalt nødpræventionsmiddel (fx en kobber-spiral). Hvis brug af kobberspiral ikke er muligt, anbefales kvinderne at fordoble den almindelige dosis levonorgestrel fra 1,5 mg til 3 mg for at kompensere for reduktionen i plasmakoncentrationen af levonorgestrel.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Meget almindelige (> 10 %) | ||
| Mave-tarm-kanalen | Kvalme | |
| Almene symptomer og reaktioner på administrationsstedet | Træthed | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Det reproduktive system og mammae | Amenoré, Underlivssmerter, Vaginalblødning | Brystspænding, Gennembrudsblødning |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Diarré, Opkastning | |
| Det reproduktive system og mammae | Dysmenoré | |
Kliniske aspekter
- Bivirkninger vil normalt være ikke-alvorlige og forbigående. Oftest forekommer kvalme (evt. opkastning), abdominal/underlivs-smerter og menstruationsforstyrrelser. Hovedpine og træthed er også almindelige.
- Overfølsomhedsreaktioner som faryngeal/ansigtsødemer og kutane reaktioner er rapporteret.
Interaktioner
- Ritonavir samt potente CYP3A4-inducerende lægemidler som fx phenytoin, carbamazepin, rifampicin, rifabutin og naturlægemidler indeholdende perikon kan øge metaboliseringshastigheden af hormonale kontraceptiva. Dette kan medføre gennembrudsblødning eller nedsat antikonceptionel virkning. Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
- Samtidig brug af lægemidler indeholdende ulipristalacetat anbefales ikke.
Graviditet
Baggrund: For brug a levenorgestrel som nødprævention er der data for 300 1. trimester-eksponerede uden tegn på overhyppighed af misdannelser. Den begrænsede datamængde tillader ikke at udelukke en øget risiko. Baseret på data for mange tusinde børn, der er blevet eksponerede for p-piller i 1. trimester, forventes ingen risiko ved at fortsætte graviditet.
Se også: Klassifikation - graviditet
Amning
Maksimal koncentration i mælken forekommer efter 2-4 timer. Den relative vægtjusterede dosis er 2 %, hvilket almindeligvis er betryggende lavt. På grund af den høje dosis bør amning dog undgås i mindst 8 timer efter indtagelsen.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Frivelle påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
Virker primært ved at hæmme ovulationen ved at undertrykke det maksimale LH-niveau, når midlet administreres før ovulation (før stigningen af LH begynder).
Farmakokinetik
- Biotilgængelighed ca. 100 %.
- Plasmahalveringstid ca. 43 timer.
- Maksimal plasmakoncentration efter 3 timer.
- Udskilles gennem nyrerne og med fæces.
- Et farmakokinetisk studie har vist, at plasmakoncentrationen reduceres med 50 % hos kvinder med overvægt (BMI > 30 kg/m2). Den kliniske relevans af disse data er uklar.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Tabletter | 1,5 mg (Orifarm Generics) |
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (HA) | tabletter
1,5 mg
(Orifarm Generics)
Frivelle |
545204 |
1 stk. (blister)
|
72,10 | 82,10 | 82,10 |
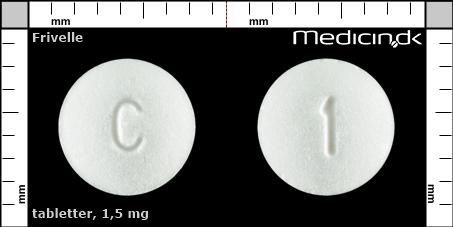
Foto og identifikation
Tabletter 1,5 mg (Orifarm Generics) |
| Præg: |
C, 1
|
| Kærv: | Ingen kærv |
| Farve: | Hvid |
| Mål i mm: | 6 x 6 |
Referencer
3800. pro.medicin.dk. 2025, https://pro.medicin.dk/ (Lokaliseret 18. marts 2026)
3801. Drugs.com. 2025, https://www.drugs.com/ (Lokaliseret 18. marts 2026)
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
4098. Charlton BM, Mølgaard-Nielsen D, Svanström H et al. Maternal use of oral contraceptives and risk of birth defects in Denmark: prospective, nationwide cohort study. BMJ. 2016, https://pubmed.ncbi.nlm.nih.gov/26738512/ (Lokaliseret 22. marts 2026)
4109. Zhang L, Chen J, Wang Y et al. Pregnancy outcome after levonorgestrel-only emergency contraception failure: a prospective cohort study. Hum Reprod. 2009; 24(7):1605-11, https://pubmed.ncbi.nlm.nih.gov/19336440/ (Lokaliseret 22. marts 2026)
4099. Wogelius P, Horváth-Puhó E, Pedersen L et al. Maternal use of oral contraceptives and risk of hypospadias - a population-based case-control study. Eur J Epidemiol. 2006; 21(10):777-81, https://pubmed.ncbi.nlm.nih.gov/17077991/ (Lokaliseret 22. marts 2026)
4100. Raman-Wilms L, Tseng AL, Wighardt S et al. Fetal genital effects of first-trimester sex hormone exposure: a meta-analysis. Obstet Gynecol. 1995; 85(1):141-9, https://pubmed.ncbi.nlm.nih.gov/7800312/ (Lokaliseret 22. marts 2026)
3802. Micromedex. , https://www.micromedexsolutions.com (Lokaliseret 18. marts 2026)
3803. Produktresumeer. http://www.produktresume.dk, http://www.ema.europa.eu, https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm, https://www.medicines.org.uk.
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



