Yderligere information
Anvendelsesområder
Arteriel hypertension hos patienter, der ikke kan behandles sufficient med monoterapi.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder:
- 20 mg olmesartanmedoxomil og 12,5 mg hydrochlorthiazid
- 20 mg olmesartanmedoxomil og 25 mg hydrochlorthiazid.
Doseringsforslag
Voksne.
- 1 tabl. 20/12,5 mg dgl. om morgenen.
- Dosis kan øges til 1 tabl. 20/25 mg dgl.
Bemærk:
- Må ikke tygges.
- Erfaring savnes vedr. børn og unge < 18 år.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-18 årErfaring savnes ved behandling af børn og unge under 18 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger ingen data.
Håndtering
Kan knuses.
Synkes hele.
Knust tablet kan opslæmmes i vand.
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på kold, blød mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
forsigtighed, monitorering |
|
|---|---|
| GFR | Advarsel |
| <30 ml/min. |
Rutinemæssig monitorering af P-kalium og P-kreatinin. |
Nedsat leverfunktion
- Højst 20 mg olmesartan ved moderat nedsat leverfunktion.
- Kontraindiceret ved stærkt nedsat leverfunktion og/eller kolestase.
Kontraindikationer
lmesartan
- Biliær obstruktion.
- Tidligere angioneurotisk ødem under behandling med angiotensin II-receptorantagonist (ARB).
- Samtidig behandling med aliskiren hos patienter med diabetes eller nedsat nyrefunktion (GFR < 60 ml/min).
Hydrochlorthiazid
- Overfølsomhed over for thiazider pga. risiko for krydsallergi.
Forsigtighedsregler
Olmesartan
- Angioødem i anamnesen
- Nyrearteriestenose
- Mitralklapstenose
- Aortastenose
- Hypertrofisk kardiomyopati.
- I forbindelse med de første doser er der hos enkelte patienter konstateret excessivt blodtryksfald, specielt ved samtidig behandling med diuretika og/eller andre vasodilatorer.
- Hypovolæmi bør korrigeres, før behandlingen indledes.
- Risiko for hyperkaliæmi ved samtidig indgift af aldosteronantagonister eller ACE-hæmmer.
- Der er indberettet intestinalt angioødem, med symptomer som mavesmerter, kvalme, opkastning og diarré der forsvandt efter seponering af angiotensin II-receptorantagonister.
Hydrochlorthiazid
- Alvorlig koronar eller cerebral arteriosklerose.
- Arthritis urica.
- Regelmæssig kontrol af elektrolytbalancen tilrådes.
- Diabetes, da hydrochlorthiazid kan øge fasteblodsukker og nedsætte glucosetolerancen.
- Forsigtighed ved alvorlig overfølsomhed for antibakterielle sulfonamider, fx sulfamethizol, sulfamethoxazol og sulfasalazin, selvom risikoen for krydsallergi er beskeden.
- Sulfonamid-afledte lægemidler som thiazider kan forårsage en idiosynkratisk reaktion, der medfører choroidal effusion med synsfeltsdefekt, forbigående myopi og akut snævervinklet glaukom. Primær behandling er øjeblikkelig seponering. Omgående medicinsk eller kirurgisk behandling bør overvejes, hvis det intraokulære tryk forbliver ukontrolleret, da ubehandlet akut snævervinklet glaukom kan føre til permanent synstab.
- Der er observeret øget risiko for non-melanom hudkræft ved langvarig brug af hydrochlorthiazid, muligvis pga. dets fotosensibiliserende virkning. Se Thiazider.
- Der er rapporteret meget sjældne, alvorlige tilfælde af akut respiratorisk distress syndrom (ARDS). Ved mistanke om ARDS bør behandling seponeres og hydrochlorthiazid bør ikke anvendes til patienter der tidligere har haft ARDS efter administration af hydrochlorthiazid.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Dyspepsi, Gastroenteritis, Obstipation | |
| Almene symptomer og reaktioner på administrationsstedet | Smerter | Træthed |
| Infektioner og parasitære sygdomme | Infektion i nedre luftveje | Influenzalignende symptomer |
| Undersøgelser | Forhøjede leverenzymer | Forhøjet plasma-kreatinkinase |
| Metabolisme og ernæring | Hypochloridæmi, Hypomagnesiæmi, Hyponatriæmi | |
| Knogler, led, muskler og bindevæv | Artritis, Knoglesmerter, Rygsmerter | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Psykiske forstyrrelser | Konfusion | |
| Nyrer og urinveje | Hæmaturi, Urinvejsinfektion | |
| Det reproduktive system og mammae | Smerter i brysterne | |
| Luftveje, thorax og mediastinum | Pharyngitis, Rhinitis | |
| Vaskulære sygdomme | Perifere ødemer | |
| Ikke almindelige (0,1-1 %) | ||
| Hjerte | Angina pectoris | Palpitationer |
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Kvalme, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed | |
| Immunsystemet | Anafylaktisk reaktion, Ansigtsødem | |
| Undersøgelser | Forhøjet ALAT/ASAT, Forhøjet gamma-glutamyltransferase - GGT, Forhøjet serum-urat | Forhøjet carbamid i blodet |
| Metabolisme og ernæring | Hypercalcæmi, Hyperglykæmi, Hyperkaliæmi, Hyperkolesterolæmi, Hyperlipidæmi, Hypertriglyceridæmi, Hypokaliæmi | Hypofagi |
| Knogler, led, muskler og bindevæv | Artralgi, Muskelkramper, Smerter i ekstremiteter | Myalgi |
| Psykiske forstyrrelser | Døsighed | |
| Det reproduktive system og mammae | Erektil dysfunktion | |
| Luftveje, thorax og mediastinum | Hoste | |
| Hud og subkutane væv | Eksem, Fotosensibilitet | Hududslæt |
| Vaskulære sygdomme | Hypotension, Ortostatisk hypotension, Synkope | |
| Sjældne (0,01-0,1 %) | ||
| Blod og lymfesystem | Agranulocytose, Anæmi, Leukopeni, Neutropeni, Trombocytopeni | |
| Hjerte | Arytmier | |
| Øjne | Synsforstyrrelser | |
| Mave-tarm-kanalen | Pancreatitis | |
| Almene symptomer og reaktioner på administrationsstedet | Letargi | Utilpashed |
| Lever og galdeveje | Icterus | |
| Immunsystemet | Angioødem, Intestinalt angioødem | Urticaria |
| Undersøgelser | Nedsat hæmatokritværdi | |
| Knogler, led, muskler og bindevæv | Kutan lupus erythematosus-lignende reaktion | |
| Benigne, maligne og uspecificerede neoplasmer | Non-melanom hudcancer | |
| Nervesystemet | Bevidsthedstab, Paræstesier | |
| Psykiske forstyrrelser | Depression | |
| Nyrer og urinveje | Akut nyresvigt, Nyrefunktionspåvirkning | |
| Luftveje, thorax og mediastinum | Dyspnø | |
| Hud og subkutane væv | Toksisk epidermal nekrolyse (TEN) | |
| Vaskulære sygdomme | Kutan vasculitis, Trombose, Vasculitis (nekrotiserende angiitis) | |
| Meget sjældne (< 0,01 %) | ||
| Luftveje, thorax og mediastinum | Akut respiratorisk distress syndrom (ARDS) (HCT) | |
| Ikke kendt hyppighed | ||
| Øjne | Choroideal effusion, Myopi (akut), Snævervinklet glaukom (akut) | |
| Lever og galdeveje | Autoimmun hepatitis | |
I meget sjældne tilfælde er der rapporteret om svær, kronisk diarré med omfattende vægttab, der muligvis skyldes en lokaliseret forsinket overfølsomhedsreaktion . Ved disse symptomer skal behandlingen seponeres, og hvis diarréen ikke forbedres i løbet af en uges tid, bør yderligere undersøgelser overvejes. Ved bekræftet sprue-lignende enteropati ved biopsi, bør behandling med olmesartanmedoxomil ikke genoptages.
Kliniske aspekter
Olmesartan
- Risiko for udtalt blodtryksfald er registreret hos patienter med stærkt aktiveret renin-angiotensin-aldosteron system, især i starten af behandling med kombinationsbehandling. Lavere startdosis kan anvendes.
- I tilfælde af angioneurotisk ødem (meget sjældent), er skift til anden angiotensin II-antagonist eller ACE-hæmmer kontraindiceret.
- Svimmelhed, hovedpine samt ortostatisk hypotension er oftest forbigående.
Hydrochlorthiazid
- Forsigtighed ved kendt arthitis urica på grund af hyperurikæmi og risiko for ny udbrud.
- Lyssensibilisering med kummulativt øget risiko for hudkræft, hvorfor kombinationspiller med hydrochlorthiazid frarådes til patienter med mere end 10 års forventet behandling
- Hyperglykæmi og impotens kan forekomme.
Interaktioner
Olmesartan
- Samtidig behandling med aliskiren hos patienter med diabetes eller nedsat nyrefunktion (GFR < 60 ml/min) kan give kraftige bivirkninger og er kontraindiceret.
- Kalium, kaliumbesparende diuretika og andre lægemidler, som øger serum-kalium kan forårsage hyperkaliæmi.
- Samtidig brug af ACE-hæmmere eller aliskiren øger risikoen for hypotension, hyperkaliæmi og nedsat nyrefunktion (inklusive akut nyresvigt). Kombinationen frarådes.
- Ved samtidig behandling med lithium kan serum-lithium øges, hvorfor kontrol af serum-lithium anbefales.
- NSAID kan svække den antihypertensive effekt.
Hydrochlorthiazid
- Samtidig indgift af colestyramin/colestipol nedsættes absorptionen af thiazider.
- Samtidig indgift af lithium kan øge serum-lithium pga. øget reabsorption af lithium i de proksimale tubuli, og monitorering anbefales.
- Virkningen af hjerteglykosider og ikke-depolariserende neuromuskulære blokkere kan forstærkes ved samtidig indgift af thiazider på grund af thiazidinduceret renalt kaliumtab.
- Risikoen for hyponatriæmi øges ved samtidig behandling med SSRI´er, andre diuretika, desmopressin, oxcarbazepin eller carbamazepin.
- Ved samtidig behandling med sotalol, kan thiazidinduceret hypokaliæmi øge risikoen for sotalolinduceret arytmi (synkope, forlænget QT).
- Kombination af kaliumtabende diuretika og NSAID kan føre til let blodtrykstigning pga. NSAID´s antidiuretiske effekt.
- På grund af nedsat udskillelse, kan serumcalcium niveauet være øget. Der anbefales monitorering af calciumniveauet før opstart af behandling med calcium tilskud, med henblik på at justere calcium dosis.
Graviditet
Baggrund:
- Olmesartan
Der er meget sparsomme data for angiotensin II-antagonister med lidt over 300 gravide eksponeret i 1. trimester af graviditeten. Der er beskrevet oligohydramnios, anuri, væksthæmning og neonatal hypotension, specielt ved eksponering i 2. og 3. trimester.
Der er ikke specifikke data for olmesartan, som tillader et meningsfyldt risikoestimat. - Hydrochlorthiazid
For hydrochlorthiazid er der data for ca. 600 1. trimester-eksponerede uden tegn på overhyppighed af misdannelser. Datamængden tillader ikke at udelukke en øget risiko.
For thiazider som gruppe er der data for mere end 2.000 eksponerede, heraf 1.000 i 1. trimester, med en let øget overhyppighed af misdannelser; i hvilket omfang disse observationer skyldes lægemiddel eller underliggende sygdom er uklart. Elektrolytforstyrrelser, hypoglykæmi, trombocytopeni og hyperbilirubinæmi hos den nyfødte har været meddelt. Behandling med diuretika kan kompromittere placentaperfusionen.
Se endvidere Hypertension hos gravide.
Se også: Klassifikation - graviditet
Amning
Bloddonor
Doping

|
Anvendelse af diuretika medfører diskvalifikation af den sportsudøvende både i og uden for konkurrence. |
Alkohol
Alkohol og Olmesartan medoxomil/hydrochlorothiazide "Krka" påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
Olmesartan
- Blokerer angiotensin-II-type 1- receptoren, hvilket resulterer i en forhøjelse af plasma-renin- og angiotensin-II-niveauerne samt nedsat aldosteron i plasma. Den kliniske effekt er universel vasodilatation uden sympatikusaktivering som ved ACE-hæmmere.
- Maksimal virkning indtræder efter ca. 8 uger.
Hydrochlorthiazid
- Thiazider hæmmer reabsorptionen af natrium og chlorid i de renale tubuli, hvilket medfører en øget, dosisafhængig udskillelse af natrium og vand. Natriuresen medfører en sekundær udskillelse af kalium og hydrogencarbonat. Den blodtryksænkende virkning skyldes initialt en reduktion i plasmavolumen og dermed i slagvolumen. Ved fortsat behandling skyldes blodtryksænkningen hovedsagelig et fald i den totale perifere vaskulære resistens.
- Virkningen indtræder efter ca. 2 timer og er maksimal efter ca. 4-6 timer.
- Virkningsvarighed ca. 12 timer.
Farmakokinetik
Olmesartanmedoxomil
- Olmesartanmedoxomil er en prodrug, som under absorptionen fra mave-tarm-kanalen hydrolyseres til den aktive substans olmesartan.
- Biotilgængelighed ca. 26 %.
- Plasmahalveringstid 10-15 timer.
- 10-16 % udskilles gennem nyrerne, resten med galden.
Hydrochlorthiazid
- Biotilgængelighed ca. 70 %.
- Plasmahalveringstid 9-13 timer.
- Udskilles hovedsageligt uomdannet gennem nyrerne.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Filmovertrukne tabletter | 20+12,5 mg |
Hydrochlorthiazid (12,5 mg)
Olmesartanmedoxomil (20 mg)
|
Farve
Andre
|
| 20+25 mg |
Hydrochlorthiazid (25 mg)
Olmesartanmedoxomil (20 mg)
|
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | filmovertrukne tabletter
20+12,5 mg
Olmesartan medox/hydrochl"Krka |
525995 |
98 stk. (blister)
|
552,75 | 5,64 | ||
| (B) | filmovertrukne tabletter
20+25 mg
Olmesartan medox/hydrochl"Krka |
168934 |
98 stk. (blister)
|
552,75 | 5,64 |
Foto og identifikation
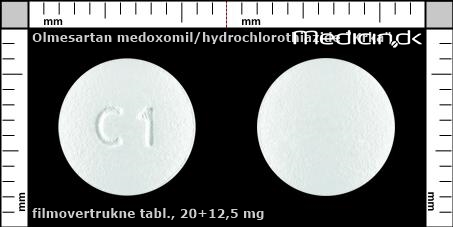
Filmovertrukne tabletter 20+12,5 mg |
| Præg: |
C1
|
| Kærv: | Ingen kærv |
| Farve: | Hvid |
| Mål i mm: | 9 x 9 |
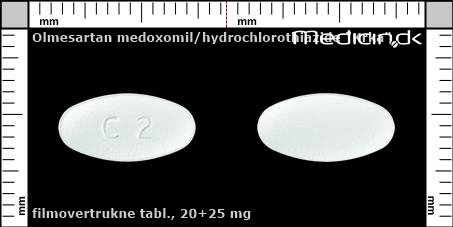
Filmovertrukne tabletter 20+25 mg |
| Præg: |
C2
|
| Kærv: | Ingen kærv |
| Farve: | Hvid |
| Mål i mm: | 6,2 x 12,2 |
Referencer
5872. Lund LC, Jensen PH, Pottegård A et al. Identifying diabetogenic drugs using real world health care databases: A Danish and Australian symmetry analysis. Diabetes Obes Metab. 2023, https://pubmed.ncbi.nlm.nih.gov/36683229/ (Lokaliseret 30. oktober 2023)
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
4332. Shimada C, Akaishi R, Cho K et al. Outcomes of 83 fetuses exposed to angiotensin receptor blockers during the second or third trimesters: a literature review. Hypertens Res. 2015; 38(5):308-13, https://pubmed.ncbi.nlm.nih.gov/25693853/ (Lokaliseret 25. marts 2026)
4329. Walfisch A, Al-maawali A, Moretti ME et al. Teratogenicity of angiotensin converting enzyme inhibitors or receptor blockers. J Obstet Gynaecol. 2011; 31(6):465-72, https://pubmed.ncbi.nlm.nih.gov/21823839/ (Lokaliseret 25. marts 2026)
4029. Rodriguez SU, Leikin SL, Hiller MC. Neonatal thombocytopenia assiciated with ante-partum administration of thiazide drugs. N Engl J Med. 1964; 270:881-4, https://pubmed.ncbi.nlm.nih.gov/14110034/ (Lokaliseret 19. marts 2026)
4030. Cuadros A, Tatum HJ. The prophylactic and therapeutic use of bendroflumethiazide in pregnancy. Am J Obstet Gynecol. 1964; 89:891-7, https://pubmed.ncbi.nlm.nih.gov/14207556/ (Lokaliseret 19. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



