Antineoplastisk middel. Proteinkinasehæmmer, JAK-hæmmer.
Anvendelsesområder
Myelofibrose
- Sygdomsrelateret splenomegali eller symptomer hos voksne, som er behandlingsnaive med JAK-hæmmere eller er blevet behandlet med ruxolitinib og som har:
- primær myelofibrose (kronisk idiopatisk myelofibrose)
- myelofibrose efter polycytaemia vera eller
- myelofibrose efter essentiel trombocytose.
Fedratinib bør kun anvendes, når behandlingen forestås af læger med særlig indsigt i maligne lidelser og behandling heraf.
Dispenseringsform
Kapsler, hårde. 1 kapsel indeholder 100 mg fedratinib.
Doseringsforslag
Voksne
- 400 mg 1 gang dgl.
- Ved behov for dosisreduktion pga. fald i thiamin-niveauer, påvirkede hæmatologiske parametre (trombocytopeni, neutropeni, anæmi), kvalme, opkastning, diarré, forhøjet ALAT/ASAT og/eller forhøjet amylase/lipase, se produktresumé.
- Under behandling skal alle patienter have profylakse med 100 mg oral thiamin dgl., og deres thiaminniveau skal vurderes.
- Dosis skal reduceres til 200 mg ved samtidig brug af potente CYP3A4-hæmmere, se Interaktioner.
Bemærk:
- Erfaring savnes vedr. børn og unge < 18 år.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-18 årErfaring savnes ved behandling af børn og unge under 18 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger ingen data.
Glemt medicin
Ved glemt dosis, skal den glemte dosis springes over.
Håndtering
Må ikke åbnes.
Synkes hele med et glas vand.
Må ikke tygges.
Kan tages med eller uden mad.
OBS: Tages til et måltid eller sammen med fedtholdige produkter for at reducere forekomsten af kvalme og opkastning.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler.
forsigtighed, erfaring savnes |
|
|---|---|
| GFR | Advarsel |
| <15 ml/min. |
Der foreligger ingen data ved GFR < 15 ml/min. |
forsigtighed, dosisjustering |
|
|---|---|
| GFR | Advarsel |
| 15-30 ml/min. |
Dosis nedsættes til 200 mg 1 gang dgl. |
Forsigtighedsregler
- Før behandlingsstart og regelmæssigt under behandlingen måles:
- Thiamin (B1-vitamin)-niveauer
- Komplet blodtælling
- Leverfunktion
- Amylase/lipase
- Carbamid og kreatinin.
- Behandling bør ikke påbegyndes hos patienter med thiaminmangel.
Bivirkninger
Dette lægemiddel har skærpet indberetningspligt. Alle eventuelle bivirkninger ved brugen skal derfor indberettes til Lægemiddelstyrelsen (Meld en bivirkning).
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Meget almindelige (> 10 %) | ||
| Blod og lymfesystem | Anæmi, Blødning, Neutropeni, Trombocytopeni | |
| Mave-tarm-kanalen | Diarré, Kvalme, Obstipation, Opkastning | |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed, Træthed | |
| Undersøgelser | Forhøjet ALAT/ASAT | Forhøjet kreatinin i blodet, Forhøjet plasma-lipase og -amylase |
| Knogler, led, muskler og bindevæv | Muskelkramper | |
| Nervesystemet | Hovedpine | |
| Nyrer og urinveje | Urinvejsinfektion | |
| Almindelige (1-10 %) | ||
| Øjne | Uveitis* | |
| Mave-tarm-kanalen | Dyspepsi | |
| Undersøgelser | Vægtøgning | |
| Knogler, led, muskler og bindevæv | Knoglesmerter, Smerter i ekstremiteter | |
| Nervesystemet | Encefalopati, Svimmelhed | |
| Nyrer og urinveje | Dysuri | |
| Vaskulære sygdomme | Hypertension | |
* Patienter med tendens til iritis/uveitis bør informeres om risikoen for at udvikle uveitis, før behandlingstart.
Interaktioner
- Dosis skal reduceres til 200 mg ved samtidig brug af potente CYP3A4-hæmmere, se tabel 2 i Elimination og cytokrom P450-systemet.
- Samtidig behandling med CYP3A4- og CYP2C19-hæmmere øger plasmakoncentrationen for fedratinib og risiko for bivirkninger (fx øger ketoconazol AUC ca. 3 gange). Evt. dosis nedjustering af fedratinib kan overvejes.
- Samtidig behandling med kraftige eller moderate CYP3A4-induktorer (fx carbamazepin, efavirenz, phenytoin, rifampicin og naturlægemidler med perikon) nedsætter plasmakoncentrationen for fedratinib (fx reducerer rifampicin og efavirenz AUC med henholdsvis 80 % og 50 %). Kombinationen bør undgås.
- Samtidig behandling med midazolam, omeprazol og metoprolol øgede AUC af midazolam, omeprazol og metoprolol med henholdsvis 4, 3, og 2 gange. Dosisjustering af disse lægemidler bør overvejes.
- Forsigtighed ved samtidig behandling med midler, der udskilles gennem nyrerne via organisk cation-transportør (OCT)2 samt multidrug og toksinekstrudering (MATE)1/2-K (fx metformin). Dosis justeres ved behov.
Graviditet
Baggrund: Der er ikke humane data for fedratinib, som tillader et meningsfyldt risikoestimat.
Enhver antineoplastisk behandling under graviditet vil være resultatet af en meget individuel og specifik vurdering af den underliggende sygdom, prognose, behandlingsalternativer og patientinvolvering. Der er ingen antineoplastiske lægemidler hvor der er kvantitative eller kvalitative humane data, som tillader et meningsfyldt risikoestimat. Generelt, på tværs af alle antineoplastiske lægemidler og de behandlede sygdomme, synes risikoen for medfødte misdannelser dog ikke væsentligt forøget. Såfremt der er behov for en detaljeret gennemgang af evidensen for det enkelte specifikke lægemiddel, anbefales kontakt til en Klinisk Farmakologisk Lægemiddelrådgivning.
Se også Antineoplastiske midler.
Se også: Klassifikation - graviditet
Fertile kvinder og mænd
Kvinder i den fertile alder skal anvende sikker antikonception under behandlingen og i mindst 1 måned efter afslutning af behandlingen.
Amning
Baggrund: På grund af virkningsmekanismen frarådes amning under behandling og i mindst 1 måned efter afslutning af behandlingen.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Inrebic® påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
- Selektiv hæmmer af Janus-associeret kinase 2 (JAK2), som formidler signalering af flere cytokiner og vækstfaktorer, som er vigtige for hæmatopoese og immunfunktion.
- Myelofibrose er relateret til dysreguleret JAK2-signalering.
Farmakokinetik
- Biotilgængelighed 63-77 %.
- Maksimal plasmakoncentration efter ca. 3 timer (ved steady-state).
- Steady-state efter 15 dage ved daglig dosering.
- Fordelingsvolumen ca. 25 l/kg.
- Plasmahaveringstid ca. 114 timer.
- Metaboliseres primært via CYP3A4 og i mindre omfang via CYP2C19.
- Udskilles primært (77 %) med fæces, en mindre mængde (5 %) udskilles gennem nyrerne.
Holdbarhed og opbevaring
Holdbarhed
Opbevares i tæt tillukket beholder for at beskytte mod fugt.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| Hårde kapsler | 100 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (BEGR) | hårde kapsler
100 mg
Inrebic |
416887 |
120 stk.
|
38.319,80 | 319,33 | 1.277,33 |
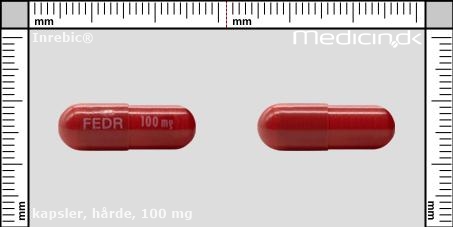
Foto og identifikation
Hårde kapsler 100 mg |
| Præg: |
FEDR, 100 mg
|
| Kærv: | Ikke relevant |
| Farve: | Rød |
| Mål i mm: | 7,7 x 21,8 |
Referencer
4264. Danet C, Araujo M, Bos-Thompson MA et al. Pregnancy outcomes in women exposed to cancer chemotherapy. Pharmacoepidemiol Drug Saf. 2018; 27(12):1302-8, https://pubmed.ncbi.nlm.nih.gov/30379378/ (Lokaliseret 25. marts 2026)
4388. de Haan J, Verheecke M, Van Calsteren K et al. Oncological management and obstetric and neonatal outcomes for women diagnosed with cancer during pregnancy: a 20-year international cohort study of 1170 patients. Lancet Oncol. 2018; 19(3):337-46, https://pubmed.ncbi.nlm.nih.gov/29395867/ (Lokaliseret 25. marts 2026)
2954. Miyamoto S, Yamada M, Kasai Y et al. Anticancer drugs during pregnancy. Jpn J Clin Oncol. 2016; 46(9):795-804, https://pubmed.ncbi.nlm.nih.gov/27284093/ (Lokaliseret 18. marts 2026)
2955. Esposito S, Tenconi R, Preti V et al. Chemotherapy against cancer during pregnancy: A systematic review on neonatal outcomes. Medicine (Baltimore). 2016; 95(38), https://pubmed.ncbi.nlm.nih.gov/27661036/ (Lokaliseret 18. marts 2026)
4268. Loibl S, Schmidt A, Gentilini O et al. Breast Cancer Diagnosed During Pregnancy: Adapting Recent Advances in Breast Cancer Care for Pregnant Patients. JAMA Oncol. 2015; 8:1145-53, https://pubmed.ncbi.nlm.nih.gov/26247818/ (Lokaliseret 25. marts 2026)
4270. Peccatori FA, Azim HA Jr, Orecchia R et al. Cancer, pregnancy and fertility: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2013, https://pubmed.ncbi.nlm.nih.gov/23813932/ (Lokaliseret 25. marts 2026)
4269. Loibl S, Han SN, von Minckwitz G et al. Treatment of breast cancer during pregnancy: an observational study. Lancet Oncol. 2012; 13(9):887-96, https://pubmed.ncbi.nlm.nih.gov/22902483/ (Lokaliseret 25. marts 2026)
2790. Azim HA Jr, Pavlidis N, Peccatori FA. Treatment of the pregnant mother with cancer: a systematic review on the use of cytotoxic, endocrine, targeted agents and immunotherapy during pregnancy. Part II: Hematological tumors. Cancer Treat Rev. 2010; 36(2):110-21, https://pubmed.ncbi.nlm.nih.gov/20018452/ (Lokaliseret 18. marts 2026)
2278. Kessler RC, Adler L, Ames M et al. The World Health Organization Adult ADHD Self-Report Scale (ASRS): a short screening scale for use in the general population. Psychol Med. 2005; 35(2):245-56, https://pubmed.ncbi.nlm.nih.gov/15841682/ (Lokaliseret 18. marts 2026)
691. Cardonick E, Iacobucci A. Use of chemotherapy during human pregnancy. Lancet Oncol. 2004; 5(5):283-91, https://pubmed.ncbi.nlm.nih.gov/15120665/ (Lokaliseret 18. marts 2026)
4267. PDQ Adult Treatment Editorial Board. Breast Cancer Treatment During Pregnancy (PDQ®): Health Professional Version. PDQ Cancer Information Summaries, National Cancer Institute (US). 2002-2017, https://pubmed.ncbi.nlm.nih.gov/26389427/ (Lokaliseret 25. marts 2026)
692. Arnon J, Meirow D, Lewis-Roness H et al. Genetic and teratogenic effects of cancer treatments on gametes and embryos. Hum Reprod Update. 2001; 7(4):394-403, https://pubmed.ncbi.nlm.nih.gov/11476352/ (Lokaliseret 18. marts 2026)
3966. SPC, EMA. European Medicines Agency. , https://www.ema.europa.eu/en/medicines (Lokaliseret 19. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



